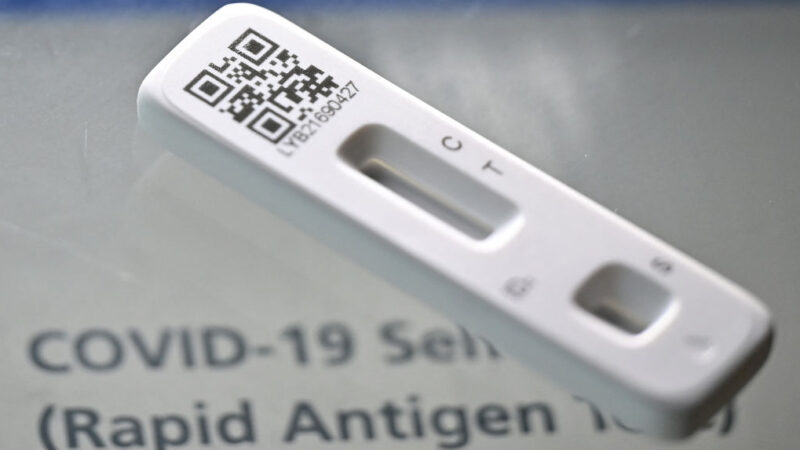
【新唐人北京时间2022年06月02日讯】在COVID-19大流行的早期,当美国第一线医疗人员急于获得关键的医疗设备时,一家德州医疗公司支付了大约50万美元,从中国购买了10万个抗体检测试剂盒。当时,只有那里在销售这些急需的产品。
然而,进口商进行产品测试后却发现,有相当数量的试剂盒是瑕疵品。尽管这些试剂2020年7月就已到货,但这些本来打算供应给美国军方及各州客户的试剂盒,却始终留在该公司的仓库。
这间公司是AnyPlace MD,现在,他们正起诉这个位于中国的卖家,希望能弥补公司的损失。
根据他们在2020年5月签订的合同,AnyPlace MD必须向安徽深蓝医疗科技有限公司(Anhui DeepBlue Medical Technology)支付75%的首付款,总额为481,125美元,剩余的118,875美元必须在到货一个月内支付。
AnyPlace MD创始人史蒂文斯(Shane Stevens)说,在收到测试盒后,他在对产品进行抽样检查时很快发现,相当数量的测试盒会出现“幽灵线”(ghost lines),并造成“假阳性”的测试结果。
在2020年7月初与合资伙伴Reliant Immune Diagnostics(诉讼中的第二名原告)的电邮中,Reliant Immune Diagnostics附上一张截图指出,美国食品和药物管理局(FDA)网站已表示,深蓝医疗科技与其它四家中国制造商生产的COVID-19测试盒已被美国监管机构标记为“不应分发”。
AnyPlace MD显然不是唯一对这家中国供应商提出投诉的公司。据当地媒体2020年4月的报导(链接),在卫生官员确定测试准确率仅为20%之后,美国国土安全部的调查人员在拉雷多市(Laredo City)查封了20,000个深蓝测试套件。
大约同一时间,中国制的瑕疵医疗用品,如口罩和试剂盒,已引起了芬兰、英国和爱尔兰等国家的反感,导致了数百万件物品被召回(链接)。2020年8月,瑞典宣布,由于中国制的检测试剂盒存在缺陷,3,700名当地民众被错误地宣判为确诊(链接)。
史蒂文斯联系了Rallo控股公司——该公司促成了他与深蓝医疗科技的交易,并要求退款。在接下来的几个月里,他一直努力试图取回近50万美元的资金。
2020年9月,当他终于与深蓝公司的代表李泽宇(Zeyu Li,音译)取得联系时,李泽宇为不能立即退款致歉,说该公司正努力确保这项产品在墨西哥或其它南美国家的销售,以确保“不会有所损失或只是小幅亏损”。
“你们为什么要把这些测试盒卖给其他人?”据史蒂文斯与《大纪元时报》分享的信息记录,他说:“它们不是好东西,会出现幽灵线,造成假阳性⋯⋯它们不是好的测试盒。”
李先生回复说,AnyPlace关于测试结果的指控“并不正确”,并说该公司只是因为美国FDA禁止分发而同意退款。
“顺便提一下,深蓝总共售出了大约1,000万组测试套件。得到了不好的结果并造成退款的,总共不足5万组⋯⋯所以我们认为,我们的产品没有大问题。”李泽宇在微信上告诉史蒂文斯。
大纪元联系了安徽深蓝医疗科技有限公司,要求其对该诉讼进行评论,但截至记者发稿时,尚未收到回复。
美国FDA虽然没有对深蓝医疗科技有限公司的产品提出具体意见,但在一封电邮中告诉大纪元,它“打算删除那些美国FDA已发出的紧急使用授权(EUA),或已通过电邮通知测试盒开发商,美国FDA将不再审查、不再签发以任何理由不再授权的测试盒”。
在2020年4月的通知(链接)中,FDA曾警告说,当时一些测试盒开发商“谎称他们的血清学测试已得到美国FDA的批准或授权,或谎称他们可诊断COVID-19”。
“FDA将对做出虚假声明或销售不准确、不可靠测试盒的公司采取适当的行动。”该机构当时说。
根据诉讼,原告表示,被告分享了一份文件,让原告误以为该测试套件是取得FDA注册的抗体测试,最终可获得FDA的批准。
AnyPlace支付的预付款,约占公司现金储备的50%。
“这对我们造成了严重伤害”,史蒂文斯说,“这使我们不得不在相当长的一段时间内停止购买COVID测试盒,同时我们也在试图收回资金。”
他说,这起诉讼(链接)是他的“最后手段”,他仍对诉讼的成功“抱持希望”。
“如果你问其他试图与中国公司打交道的人,他们可能会说成功的可能性很小。但很多时候,我只需要做我认为正确的事情。”史蒂文斯说。
“我心想,如果是其它一些没有资源的公司遇上这种事该怎么办?如果一些公司付出所有资源试图从他们(中国公司)那里买东西呢?这将使那间公司破产。”他说。
“这种公司的存在是很危险的⋯⋯所以我觉得不管结果如何,我都有义务去做。”史蒂文斯说。
(转自大纪元/责任编辑:陈北晨)